Понятие химического равновесия
Равновесным считается состояние системы, которое остается неизменным, причем это состояние не обусловлено действием каких-либо внешних сил. Состояние системы реагирующих веществ, при котором скорость прямой реакции становится равной скорости обратной реакции, называется химическим равновесием . Такое равновесие называется еще подвижны м или динамическим равновесием.
Признаки химического равновесия
1. Состояние системы остается неизменным во времени при сохранении внешних условий.
2. Равновесие является динамическим, то есть обусловлено протеканием прямой и обратной реакции с одинаковыми скоростями.
3. Любое внешнее воздействие вызывает изменение в равновесии системы; если внешнее воздействие снимается, то система снова возвращается в исходное состояние.
4. К состоянию равновесия можно подойти с двух сторон – как со стороны исходных веществ, так и со стороны продуктов реакции.
5. В состоянии равновесия энергия Гиббса достигает своего минимального значения.
Принцип Ле Шателье
Влияние изменения внешних условий на положение равновесия определяется принципом Ле Шателье (принципом подвижного равновесия): если на систему, находящуюся в состоянии равновесия, производить какое–либо внешнее воздействие, то в системе усилится то из направлений процесса, которое ослабляет эффект этого воздействия, и положение равновесия сместится в том же направлении.
Принцип Ле Шателье применим не только к химическим процессам, но и к физическим, таким как кипение, кристаллизация, растворение и т. д.
Рассмотрим влияние различных факторов на химическое равновесие на примере реакции окисления NO:
2 NO (г) + O 2(г) 2 NO 2(г) ; H о 298 = - 113,4 кДж/моль.
Влияние температуры на химическое равновесие
При повышении температуры равновесие сдвигается в сторону эндотермической реакции, при понижении температуры – в сторону экзотермической реакции.
Степень смещения равновесия определяется абсолютной величиной теплового эффекта: чем больше по абсолютной величине энтальпия реакции H, тем значительнее влияние температуры на состояние равновесия.
В рассматриваемой реакции синтеза оксида азота (IV) повышение температуры сместит равновесие в сторону исходных веществ.
Влияние давления на химическое равновесие
Сжатие смещает равновесие в направлении процесса, который сопровождается уменьшением объема газообразных веществ, а понижение давления сдвигает равновесие в противоположную сторону. В рассматриваемом примере в левой части уравнения находится три объема, а в правой – два. Так как увеличение давления благоприятствует процессу, протекающему с уменьшением объема, то при повышении давления равновесие сместится вправо, т.е. в сторону продукта реакции – NO 2 . Уменьшение давления сместит равновесие в обратную сторону. Следует обратить внимание на то, что, если в уравнении обратимой реакции число молекул газообразных веществ в правой и левой частях равны, то изменение давления не оказывает влияния на положение равновесия.
Влияние концентрации на химическое равновесие
Для рассматриваемой реакции введение в равновесную систему дополнительных количеств NO или O 2 вызывает смещение равновесия в том направлении, при котором концентрация этих веществ уменьшается, следовательно, происходит сдвиг равновесия в сторону образования NO 2 . Увеличение концентрации NO 2 смещает равновесие в сторону исходных веществ.
Катализатор одинаково ускоряет как прямую, так и обратную реакции и поэтому не влияет на смещение химического равновесия.
При введении в равновесную систему (при Р = const) инертного газа концентрации реагентов (парциальные давления) уменьшаются. Поскольку рассматриваемый процесс окисления NO идет с уменьшением объема, то при добавлении ин
Константа химического равновесия
Для химической реакции:
2 NO (г) + O 2(г) 2 NO 2(г)
константа химической реакции К с есть отношение:
 (12.1)
(12.1)
В этом уравнении в квадратных скобках – концентрации реагирующих веществ, которые устанавливаются при химическом равновесии, т.е. равновесные концентрации веществ.
Константа химического равновесия связана с изменением энергии Гиббса уравнением:
G T о = – RTlnK . (12.2).
Примеры решения задач
При некоторой температуре равновесные концентрации в системе 2CO (г) + O 2 (г) 2CO 2 (г) составляли: = 0,2 моль/л, = 0,32 моль/л, = 0,16 моль/л. Определить константу равновесия при этой температуре и исходные концентрации CO и O 2 , если исходная смесь не содержала СО 2 .![]() .
.
2CO (г) + O 2(г) 2CO 2(г).
Во второй строке под с прореагир понимается концентрация прореагировавших исходных веществ и концентрация образующегося CO 2 , причем, с исходн = с прореагир + с равн .
Используя справочные данные, рассчитать константу равновесия процесса3 H 2 (Г) + N 2 (Г) 2 NH 3 (Г) при 298 К.
G 298 о = 2·(- 16,71) кДж = -33,42·10 3 Дж.
G T о = - RTlnK.
lnK = 33,42·10 3 /(8,314× 298) = 13,489. K = 7,21× 10 5 .
Определить равновесную концентрацию HI в системеH 2(г) + I 2(г) 2HI (г) ,
если при некоторой температуре константа равновесия равна 4, а исходные концентрации H 2 , I 2 и HI равны, соответственно, 1, 2 и 0 моль/л.
Решение. Пусть к некоторому моменту времени прореагировало x моль/л H 2.
![]() .
.
Решая это уравнение, получаем x = 0,67.
Значит, равновесная концентрация HI равна 2× 0,67 = 1,34 моль/л.
Используя справочные данные, определить температуру, при которой константа равновесия процесса: H 2(г) + HCOH (г) CH 3 OH (г) становится равной 1. Принять, что Н о Т » Н о 298 , а S о T » S о 298 .Если К = 1, то G о T = - RTlnK = 0;
G о T » Н о 298 - ТD S о 298 . Тогда ;
Н о 298 = -202 – (- 115,9) = -86,1 кДж = - 86,1× 10 3 Дж;
S о 298 = 239,7 – 218,7 – 130,52 = -109,52 Дж/К;
![]() К.
К.
Решение. Пусть к некоторому моменту времени прореагировало x моль/л SO 2.
SO 2(Г) + Cl 2(Г) SO 2 Cl 2(Г)
Тогда получаем:
![]() .
.
Решая это уравнение, находим: x 1 = 3 и x
2 = 1,25. Но x
1 = 3 не удовлетворяет условию задачи.
Следовательно, = 1,25 + 1 = 2,25 моль/л.
Задачи для самостоятельного решения
12.1. В какой из приведенных реакций повышение давления сместит равновесие вправо? Ответ обосновать.
1) 2 NH 3 (г) 3 H 2 (г) + N 2 (г)
2) ZnCO 3 (к) ZnO (к) + CO 2 (г)
3) 2HBr (г) H 2 (г) + Br 2 (ж)
4) CO 2 (г) + C (графит) 2CO (г)
12.2. При некоторой температуре равновесные концентрации в системе
2HBr (г) H 2 (г) + Br 2 (г)
составляли: = 0,3 моль/л, = 0,6 моль/л, = 0,6 моль/л. Определить константу равновесия и исходную концентрацию HBr.
12.3. Для реакции H 2(г) + S (г) H 2 S (г) при некоторой температуре константа равновесия равна 2. Определить равновесные концентрации H 2 и S, если исходные концентрации H 2 , S и H 2 S равны, соответственно, 2, 3 и 0 моль/л.
Константа химического равновесия
Количественной характеристикой химического равновесия является константа равновесия , которая может быть выражена через равновесные концентрации С i , парциальные давления P i или мольные доли X i реагирующих веществ. Для некоторой реакции
соответствующие константы равновесия выражаются следующим образом:



Константа равновесия есть характерная величина для каждой обратимой химической реакции; величина константы равновесия зависит только от природы реагирующих веществ и температуры. На основании уравнения состояния идеального газа, записанного в виде соотношения P i = C i RT, где С i = n i /V, и закона Дальтона для идеальной газовой смеси, выраженного уравнением P = ΣP i , можно вывести соотношения между парциальным давлением P i , молярной концентрацией С i и мольной долей X i i-го компонента:
![]()
Отсюда получаем соотношение между K c , K p и K x:
![]()
Здесь Δν – изменение числа молей газообразных веществ в течение реакции:
Δν = – ν 1 – ν 2 – ... + ν" 1 + ν" 2 + ...
Величина константы равновесия K x , в отличие от констант равновесия K c и K p , зависит от общего давления Р.
Выражение для константы равновесия элементарной обратимой реакции может быть выведено из кинетических представлений. Рассмотрим процесс установления равновесия в системе, в которой в начальный момент времени присутствуют только исходные вещества. Скорость прямой реакции V 1 в этот момент максимальна, а скорость обратной V 2 равна нулю:
![]()
![]()
По мере уменьшения концентрации исходных веществ растет концентрация продуктов реакции; соответственно, скорость прямой реакции уменьшается, скорость обратной реакции увеличивается. Очевидно, что через некоторое время скорости прямой и обратной реакции сравняются, после чего концентрации реагирующих веществ перестанут изменяться, т.е. установится химическое равновесие.
Приняв, что V 1 = V 2 , можно записать:

Т.о., константа равновесия есть отношение констант скорости прямой и обратной реакции. Отсюда вытекает физический смысл константы равновесия: она показывает, во сколько раз скорость прямой реакции больше скорости обратной при данной температуре и концентрациях всех реагирующих веществ, равных 1 моль/л. Приведённый вывод выражения для константы равновесия, однако, исходит из ложной в общем случае посылки, что скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам. Как известно, в общем случае показатели степени при концентрациях реагентов в кинетическом уравнении химической реакции не совпадают со стехиометрическими коэффициентами.
11. Окислительно-восстановительные реакции: определение, основные понятия, сущность окисления и восстановления, важнейшие окислители и восстановители реакции.
Окислительно-восстановительными называют процессы, которые, сопровождаются смещением электронов от одних свободных или связанных атомов к другим. Поскольку в таких случаях имеет значение не степень смещения, а только число смещенных электронов, то принято условно считать смещение всегда полным и говорить об отдаче или смещении электронов.
Если атом или ион элемента отдает или принимает электроны, то в первом случае степень окисления элемента повышается, и он переходит в окисленную форму (ОФ), а во втором – понижается, и элемент переходит в восстановленную форму (ВФ). Обе формы составляют сопряженную окислительно-восстановительную пару. В каждой окислительно-восстановительной реакции участвуют две сопряженные пары. Одна из них соответствует переходу окислителя, принимающего электроны, в его восстановленную форму (ОФ 1 →ВФ 1), а другая – переходу восстановителя, отдающего электроны, в его окисленную форму (ВФ 2 →ОФ 2), например:
Cl 2 + 2 I – → 2 Cl – + I 2
ОФ 1 ВФ 1 ВФ 2 ОФ 2
(здесь Cl 2 – окислитель, I – – восстановитель)
Таким образом, одна и та же реакция всегда является одновременно процессом окисления восстановителя и процессом восстановления окислителя.
Коэффициенты в уравнениях окислительно-восстановительных реакций могут быть найдены методами электронного баланса и электронно-ионного баланса. В первом случае число принятых или отданных электронов определяется по разности степеней окисления элементов в исходном и конечном состояниях. Пример:
HN 5+ O 3 + H 2 S 2– → N 2+ O + S + H 2 O
В этой реакции степень окисления меняют два элемента: азот и сера. Уравнения электронного баланса:
Доля диссоциированных молекул H 2 S незначительна, поэтому в уравнение подставляется не ион S 2– , а молекула H 2 S. Вначале уравнивается баланс частиц. При этом в кислой среде для уравнивания используются ионы водорода, добавляемые к окисленной форме, и молекулы воды, добавляемые к восстановленной форме. Затем уравнивается баланс зарядов, и справа от черты указываются коэффициенты, уравнивающие количество отданных и принятых электронов. После этого внизу записывается суммарное уравнение с учетом коэффициентов:
Получили сокращенное ионно-молекулярное уравнение. Добавив к нему ионы Na + и K + , получим аналогичное уравнение в полной форме, а также молекулярное уравнение:
NaNO 2 + 2 KMnO 4 + 2 KOH → NaNO 3 + 2 K 2 MnO 4 + H 2 O
В нейтральной среде баланс частиц уравнивается путем добавления молекул воды в левую часть полуреакций, а в правую часть добавляются ионы H + или OH – :
I 2 + Cl 2 + H 2 O → HIO 3 + HCl
Исходные вещества не являются кислотами или основаниями, поэтому в начальный период протекания реакции среда в растворе близка к нейтральной. Уравнения полуреакций:
| I 2 + 6 H 2 O + 10e → 2 IO 3 – + 12 H + | |
| Cl 2 + 2e → 2 Cl – | |
| I 2 + 5 Cl 2 + 6 H 2 O → 2 IO 3 – + 12 H + + 10 Cl – |
Уравнение реакции в молекулярной форме:
I 2 + 5 Cl 2 + 6 H 2 O → 2 HIO 3 + 10 HCl.
ВАЖНЕЙШИЕ ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ. КЛАССИФИКАЦИЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ
Пределы окисления и восстановления элемента выражаются максимальным и минимальным значениями степеней окисления *. В этих крайних состояниях, определяемых положением в таблице Менделеева, элемент имеет возможность проявить только одну функцию – окислителяили восстановителя. Соответственно и вещества, содержащие элементы в этих степенях окисления, являются только окислителями (HNO 3 , H 2 SO 4 ,HClO 4 , KMnO 4 , K 2 Cr 2 O 7 и др.) или только восстановителями (NH 3 , H 2 S, галогеноводороды, Na 2 S 2 O 3 и др.). Вещества, содержащие элементы в промежуточных степенях окисления, могут быть как окислителями, так и восстановителями (HClO, H 2 O 2 , H 2 SO 3 и др.).
Окислительно-восстановительные реакции разделяются на три основных типа: межмолекулярные, внутримолекулярные и реакции диспропорционирования.
К первому типу относятся процессы, в которых атомы элемента-окислителя и элемента-восстановителя входят в состав разных молекул.
Внутримолекулярными называются реакции, в которых окислитель и восстановитель в виде атомов разных элементов находятся в составе одной и той же молекулы. Например, термическое разложение хлората калия по уравнению:
2 KClO 3 → 2 KCl + 3 O 2
Реакциями диспропорционирования называют процессы, в которых окислителем и восстановителем является один и тот же элемент в одной и той же степени окисления, которая в реакции одновременно как снижается, так и повышается, например:
3 HClO → HClO 3 + 2 HCl
Возможны также реакции обратного диспропорционирования. К ним относятся внутримолекулярные процессы, в которых окислителем и восстановителем является один и тот же элемент, но в виде атомов, находящихся в разной степени окисления и выравнивающих ее в результате реакции, например.
Константа химического равновесия
Большинство химических реакций обратимы, т.е. протекают одновременно в противоположных направлениях. В тех случаях, когда прямая и обратная реакции идут с одинаковой скоростью, наступает химическое равновесие. Например, в обратимой гомогенной реакции: H 2 (г) + I 2 (г) ↔ 2HI(г) соотношение скоростей прямой и обратной реакций согласно закону действующих масс зависит от соотношения концентраций реагирующих веществ, а именно: скорость прямой реакции: υ 1 = k 1 [Н 2 ]. Скорость обратной реакции: υ 2 = k 2 2 .
Если H 2 и I 2 – исходные вещества, то в первый момент скорость прямой реакции определяется их начальными концентрациями, а скорость обратной реакции равна нулю. По мере израсходования H 2 и I 2 и образования HI скорость прямой реакции уменьшается, а скорость обратной реакции возрастает. Спустя некоторое время обе скорости уравниваются, и в системе устанавливается химическое равновесие, т.е. число образующихся и расходуемых молекул HI в единицу времени становится одинаковым.
Так как при химическом равновесии скорости прямой и обратной реакций равны V 1 = V 2 , то k 1 = k 2 2 .
Поскольку k 1 и k 2 при данной температуре постоянны, то их отношение будет постоянным. Обозначая его через K, получим:

К – называется константой химического равновесия, а приведенное уравнение – законом действующих масс (Гульдберга - Ваале).
В общем случае для реакции вида аА+bB+…↔dD+eE+… константа равновесия равна ![]() . Для взаимодействия между газообразными веществами часто пользуются выражением , в котором реагенты представлены равновесными парциальными давлениями p. Для упомянутой реакции
. Для взаимодействия между газообразными веществами часто пользуются выражением , в котором реагенты представлены равновесными парциальными давлениями p. Для упомянутой реакции  .
.
Состояние равновесия характеризует тот предел, до которого в данных условиях реакция протекает самопроизвольно (∆G<0). Если в системе наступило химическое равновесие, то дальнейшее изменение изобарного потенциала происходить не будет, т.е. ∆G=0.
Соотношение между равновесными концентрациями не зависит от того, какие вещества берутся в качестве исходных (например, H 2 и I 2 или HI), т.е. к состоянию равновесия можно подойти с обеих сторон.
Константа химического равновесия зависит от природы реагентов и от температуры; от давления (если оно слишком высокое) и от концентрации реагентов константа равновесия не зависит.
Влияние на константу равновесия температуры, энтальпийного и энтропийного факторов . Константа равновесия связана с изменением стандартного изобарно-изотермического потенциала химической реакции ∆G o простым уравнением ∆G o =-RT ln K.
Из него видно, что большим отрицательным значениям ∆G o (∆G o <<0) отвечают большие значения К, т.е. в равновесной смеси преобладают продукты взаимодействия. Если же ∆G o характеризуется большими положительными значениями (∆G o >>0), то в равновесной смеси преобладают исходные вещества. Указанное уравнение позволяет по величине ∆G o вычислить К, а затем и равновесные концентрации (парциальные давления) реагентов. Если учесть, что ∆G o =∆Н o -Т∆S o , то после некоторого преобразования получим ![]() . Из этого уравнения видно, что константа равновесия очень чувствительна к изменению температуры. Влияние на константу равновесия природы реагентов определяет ее зависимость от энтальпийного и энтропийного факторов.
. Из этого уравнения видно, что константа равновесия очень чувствительна к изменению температуры. Влияние на константу равновесия природы реагентов определяет ее зависимость от энтальпийного и энтропийного факторов.
Задание 135.
Вычислите константу равновесия для гомогенной системы
если равновесие концентрации реагирующих веществ (молы/л):
[СО]
Р = 0,004; [Н
2 О]
Р = 0,064; [СО
2 ]
Р = 0,016; [Н
2 ]
р = 0,016,
Чему равны исходные концентрации воды и СО? Ответ: К = 1; исх = 0,08 моль/л; [СО]исх =0, 02 моль/л.
Решение:
Уравнение реакции имеет вид:
СО (г) + Н 2 О (г) СО 2 (г) + Н2 (г)
Константа уравнения данной реакции имеет выражение:
Для нахождения исходных концентраций веществ Н 2 О и СО учтём, что согласно уравнению реакции из 1 моль СО и 1 моль Н 2 О образуется 1 моль СО 2 и 1 моль Н 2 . Поскольку по условию задачи в каждом литре системы образовалось 0,016 моль СО 2 и 0,016 моль Н 2 , то при этом было израсходовано по 0,016 моль СО и Н 2 О. Таким образом, искомые исходные концентрации равны:
Исх = [Н 2 О] Р + 0,016 = 0,004 + 0,016 = 0,02 моль/л;
[СО] исх = [СО] Р + 0,016 = 0,064 + 0,016 = 0, 08 моль/л.
Ответ: Кp = 1; исх = 0,08 моль/л; [СО] исх =0, 02 моль/л.
Задание 136.
Константа равновесия гомогенной системы
при некоторой температуре равна 1. Вычислите равновесные концентрации всех реагирующих веществ, если исходные концентрации равны (молы/л): [СО] исх = 0,10; [Н 2 О] исх = 0,40.
Ответ: [СО 2 ] Р = [Н 2 ] Р = 0,08; [СO] P = 0,02; [Н 2 O] P = 0,32.
Решение:
Уравнение реакции имеет вид:
СО (г) + Н 2 О (г) СО 2 (г) + Н 2 (г)
При равновесии скорости прямой и обратной реакций равны, а отношение констант этих скоростей постоянно и называется константой равновесия данной системы:

Обозначаем за х моль/л равновесную концентрацию одного из продуктов реакции, тогда равновесная концентрация другого будет также х моль/л так как они оба образуются в одинаковом количестве. Равновесные концентрации исходных веществ будут:
[СО] исх = 0,10 – х моль/л; [Н 2 О] исх = 0,40 - х моль/л. (так как на образование х моль/л продукта реакции расходуется соответственно по х моль/л СО и Н 2 О. В момент равновесия концентрация всех веществ будет (моль/л): [СО 2 ] Р = [Н 2 ] Р = х; [СO] P = 0,10 - х; [Н 2 O] P = 0,4 – х.
Подставляем эти значения в выражение константы равновесия:
![]()
Решая уравнение, находим х = 0,08. Отсюда равновесие концентрации (моль/л):
[СО 2 ] Р = [Н 2 ] Р = х = 0,08 моль/л;
[Н 2 O] P = 0,4 – х = 0,4 – 0.08 = 0,32 моль/л;
[СO] P = 0,10 – х = 0,10 – 0,08 = 0,02 моль/л.
Задание 137.
Константа равновесия гомогенной системы N 2 + ЗН 2 = 2NH 3 при некоторой температуре равна 0,1. Равновесные концентрации водорода и аммиака соответственно равны 0,2 и 0,08 моль/л. Вычислите равновесную и исходную концентрации азота. Ответ: P = 8 молы/л; исх = 8,04 моль/л.
Решение:
Уравнение реакции имеет вид:
N 2 + ЗН 2 = 2NH 3
Обозначим равновесную концентрацию N2 через х моль/л. Выражение константы равновесия данной реакции имеет вид:

Подставим в выражение константы равновесия данные задачи и найдём концентрацию N 2

Для нахождения исходной концентрации N 2 , учтём, что, согласно уравнению реакции на образование 1 моль NH 3 затрачивается ½ моль N 2 . Поскольку по условию задачи в каждом литре системы образовалось 0,08 моль NH 3 , то при этом было израсходовано 0,08 . 1/2 = 0,04 моль N 2 . Таким образом, искомая исходная концентрация N 2 равна:
Исх = P + 0,04 = 8 + 0,04 = 8,04 моль/л.
Ответ: P = 8 молы/л; исх = 8,04 моль/л.
Задание 138
При некоторой температуре равновесие гомогенной системы
2NО + O 2 ↔ 2NO 2 установилось при следующих концентрациях реагирующих веществ (молы/л): p = 0,2; [О 2 ] р = 0,1; р = 0,1. Вычислите константу равновесия и исходную концентрацию NO и O 2 . Ответ: К = 2,5; исх = 0,3 молы/л; [О 2 ] ис х = 0,15 моль/л.
Решение:
Уравнение реакции:
2NО + O 2 ↔ 2NO 2

Для нахождения исходных концентраций NO и O 2 учтём, что согласно уравнению реакции, из 2 моль NO и 1 моль О2 образуется 2 моль NO 2 , то при этом было затрачено 0,1 моль NO и 0,05 моль О 2 . Таким образом, исходные концентрации NO и О 2 равны:
Исх = NО] p + 0,1 = 0,2 + 0,1 = 0,3 молы/л;
[О 2 ] исх = [О 2 ] р + 0,05 = 0,1 + 0,05 = 0,15 моль/л.
Ответ: Кp = 2,5; исх = 0,3 молы/л; [О 2 ] исх = 0,15 моль/л.
Задание 139.
Почему при изменении давления смещается равновесие системы
N 2 + 3Н 2 ↔ 2NH 3 и, не смещается равновесие системы N 2 + O 2 2NO? Ответ мотивируйте на основании расчета скорости прямой и обратной реакций в этих системах до и после изменения давления. Напишите выражения для констант равновесия каждой из данных систем.
Решение:
а) Уравнение реакции:
N 2 + 3Н 2 ↔ 2NH 3 .
Из уравнения реакции следует, что реакция протекает с уменьшением объёма в системе (из 4 моль газообразных веществ образуется 2 моль газообразного вещества). Поэтому при изменении давления в системе будут наблюдаться смещение равновесия. Если повысить давление в данной системе, то, согласно принципу Ле Шателье, равновесие сместится вправо, в сторону уменьшения объёма. При смещении равновесия в системе вправо скорость прямой реакции будет больше скорости обратной реакции:
пр >обр или пр = k 3 > о бр = k 2 .
Если же давление в системе уменьшить, то равновесие системы сместится влево, в сторону увеличения объёма, то при смещении равновесия влево скорость прямой реакции будет меньше, чем скорость прямой:
пр < обр или (пр = k 3 )< (обр = k 2).
б) Уравнение реакции:
N2 + O2) ↔ 2NO. .
Из уравнения реакции следует, что при протекание реакции не сопровождается изменением объёма, реакция протекает без изменения числа молей газообразных веществ. Поэ му изменение давления в системе не приведёт к смещению равновесия, поэтому скорости прямой и обратной реакции будут равны:
пр = обр = или (пр k [О 2 ]) = (обр = k 2) .
Задание 140.
Исходные концентрации исх и [С1 2 ]исх в гомогенной системе
2NO + Сl 2 ↔ 2NOС1 составляют соответственно 0,5 и 0,2 моль/л. Вычислите константу равновесия, если к моменту наступления равновесия прореагировало 20% NО. Ответ: 0,417.
Решение:
Уравнение реакции имеет вид: 2NO + Сl 2 ↔ 2NOС1
Согласно условию задачи в реакцию вступило 20% NO, что составляет 0,5 .
0,2 = 0,1 моль, а не прореагировало 0,5 – 0,1 = 0,4 моль NO. Из уравнения реакции следует, что на каждые 2 моль NO расходуется 1 моль Cl2, при этом образуется 2 моль NOCl. Следовательно, c 0,1 моль NO в реакцию вступило 0,05 моль Cl 2 и образовалось 0,1 моль NOCl. Осталось не израсходованным 0,15 моль Cl 2 (0,2 – 0,05 = 0,15). Таким образом, равновесные концентрации, участвующих веществ равны (моль/л):
Р = 0,4; p = 0,15; р = 0,1.
Константа равновесия данной реакции выражается уравнением:
![]()
Подставляя в данное выражение равновесные концентрации веществ, получим.
Химическим равновесием называется такое состояние обратимой химической реакции
aA + b B = c C + d D,
при котором с течением времени не происходит изменения концентраций реагирующих веществ в реакционной смеси. Состояние химического равновесия характеризуется константой химического равновесия :
где C i – концентрации компонентов в равновесной идеальной смеси.
Константа равновесия может быть выражена также через равновесные мольные доли X i компонентов:
Для реакций, протекающих в газовой фазе, константу равновесия удобно выражать через равновесные парциальные давления P i компонентов:
Для идеальных газов P i = C i RT и P i = X i P , где P – общее давление, поэтому K P , K C и K X связаны следующим соотношением:
K P = K C (RT) c+d–a–b = K X P c+d–a–b . (9.4)
Константа равновесия связана с r G o химической реакции:
![]() (9.5)
(9.5)
![]() (9.6)
(9.6)
Изменение r G или r F в химической реакции при заданных (не обязательно равновесных) парциальных давлениях P i или концентрациях C i компонентов можно рассчитать по уравнению изотермы химической реакции (изотермы Вант-Гоффа ):
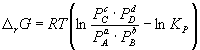 . (9.7)
. (9.7)
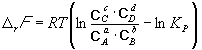 . (9.8)
. (9.8)
Согласно принципу Ле Шателье , если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится так, чтобы уменьшить эффект внешнего воздействия. Так, повышение давления сдвигает равновесие в сторону уменьшения количества молекул газа. Добавление в равновесную смесь какого-либо компонента реакции сдвигает равновесие в сторону уменьшения количества этого компонента. Повышение (или понижение) температуры сдвигает равновесие в сторону реакции, протекающей с поглощением (выделением) теплоты.
Количественно зависимость константы равновесия от температуры описывается уравнением изобары химической реакции (изобары Вант-Гоффа )
![]() (9.9)
(9.9)
и изохоры химической реакции (изохоры Вант-Гоффа )
![]() . (9.10)
. (9.10)
Интегрирование уравнения (9.9) в предположении, что r H реакции не зависит от температуры (что справедливо в узких интервалах температур), дает:
![]() (9.11)
(9.11)
![]() (9.12)
(9.12)
где C – константа интегрирования. Таким образом, зависимость ln K P от 1/Т должна быть линейной, а наклон прямой равен – r H /R .
Интегрирование в пределах K 1 , K 2 , и T 1, T 2 дает:
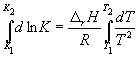 (9.13)
(9.13)
 (9.14)
(9.14)
По этому уравнению, зная константы равновесия при двух разных температурах, можно рассчитать r H реакции. Соответственно, зная r H реакции и константу равновесия при одной температуре, можно рассчитать константу равновесия при другой температуре.
ПРИМЕРЫ
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K. f G o для CO(г) и CH 3 OH(г) при 500 К равны –155.41 кДж. моль –1 и –134.20 кДж. моль –1 соответственно.
Решение. G o реакции:
r G o = f G o (CH 3 OH) – f G o (CO) = –134.20 – (–155.41) = 21.21 кДж. моль –1 .
![]() = 6.09 10 –3 .
= 6.09 10 –3 .
Пример 9-2. Константа равновесия реакции
равна K P = 1.64 10 –4 при 400 o C. Какое общее давление необходимо приложить к эквимолярной смеси N 2 и H 2 , чтобы 10% N 2 превратилось в NH 3 ? Газы считать идеальными.
Решение. Пусть прореагировало моль N 2 . Тогда
| N 2 (г) | + | 3H 2 (г) | = | 2NH 3 (г) | |
| Исходное количество | 1 | 1 | |||
| Равновесное количество | 1– | 1–3 | 2 (Всего: 2–2) | ||
| Равновесная мольная доля: |
Следовательно, K
X = 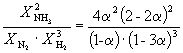 и K P = K X . P
–2
=
и K P = K X . P
–2
=  .
.
Подставляя = 0.1 в полученную формулу, имеем
1.64 10 –4 =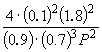 , откуда P
= 51.2 атм.
, откуда P
= 51.2 атм.
Пример 9-3. Константа равновесия реакции
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K равна K P = 6.09 10 –3 . Реакционная смесь, состоящая из 1 моль CO, 2 моль H 2 и 1 моль инертного газа (N 2) нагрета до 500 K и общего давления 100 атм. Рассчитать состав равновесной смеси.
Решение. Пусть прореагировало моль CO. Тогда
| CO(г) | + | 2H 2 (г) | = | CH 3 OH(г) | |
| Исходное количество: | 1 | 2 | 0 | ||
| Равновесное количество: | 1– | 2–2 | |||
| Всего в равновесной смеси: | 3–2 моль компонентов + 1 моль N 2 = 4–2 моль | ||||
| Равновесная мольная доля | |||||
Следовательно, K
X = 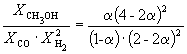 и K P = K X . P –2
=
и K P = K X . P –2
= ![]() .
.
Таким образом, 6.09 10 –3
= ![]() .
.
Решая это уравнение, получаем = 0.732. Соответственно, мольные доли веществ в равновесной смеси равны: = 0.288, = 0.106, = 0.212 и = 0.394.
Пример 9-4. Для реакции
N 2 (г) + 3H 2 (г) = 2NH 3 (г)
при 298 К K P = 6.0 10 5 , а f H o (NH 3) = –46.1 кДж. моль –1 . Оценить значение константы равновесия при 500 К.
Решение. Стандартная мольная энтальпия реакции равна
r H o = 2 f H o (NH 3) = –92.2 кДж. моль –1 .
Согласно уравнению (9.14),  =
=
Ln (6.0 10 5) + ![]() = –1.73, откуда K
2 =
0.18.
= –1.73, откуда K
2 =
0.18.
Отметим, что константа равновесия экзотермической реакции уменьшается с ростом температуры, что соответствует принципу Ле Шателье.
ЗАДАЧИ
- При 1273 К и общем давлении 30 атм в равновесной смеси
- При 2000 o C и общем давлении 1 атм 2% воды диссоциировано на водород и кислород. Рассчитать константу равновесия реакции
- Константа равновесия реакции
- Константа равновесия реакции
- Сосуд объемом 3 л, содержащий 1.79 10 –2 моль I 2 , нагрели до 973 K. Давление в сосуде при равновесии оказалось равно 0.49 атм. Считая газы идеальными, рассчитать константу равновесия при 973 K для реакции
- Для реакции
- Для реакции
- Сосуд объемом 1 л, содержащий 0.341 моль PCl 5 и 0.233 моль N 2 , нагрели до 250 o C. Общее давление в сосуде при равновесии оказалось равно 29.33 атм. Считая все газы идеальными, рассчитать константу равновесия при 250 o C для протекающей в сосуде реакции
- Константа равновесия реакции
- При 25 o C f G o (NH 3) = –16.5 кДж. моль –1 . Рассчитать r G реакции образования NH 3 при парциальных давлениях N 2 , H 2 и NH 3 , равных 3 атм, 1 атм и 4 атм соответственно. В какую сторону реакция будет идти самопроизвольно при этих условиях?
- Экзотермическая реакция
- Константа равновесия газофазной реакции изомеризации борнеола (C 10 H 17 OH) в изоборнеол равна 0.106 при 503 K. Смесь 7.5 г борнеола и 14.0 г изоборнеола поместили в сосуд объемом 5 л и выдерживали при 503 K до достижения равновесия. Рассчитать мольные доли и массы борнеола и изоборнеола в равновесной смеси.
- Равновесие в реакции
- Рассчитать общее давление, которое необходимо приложить к смеси 3 частей H 2 и 1 части N 2 , чтобы получить равновесную смесь, содержащую 10% NH 3 по объему при 400 o C. Константа равновесия для реакции
- При 250 o C и общем давлении 1 атм PCl 5 диссоциирован на 80% по реакции
- При 2000 o C для реакции
- Рассчитать стандартную энтальпию реакции, для
которой константа равновесия
а) увеличивается в 2 раза, б) уменьшается в 2 раза при изменении температуры от 298 К до 308 К. - Зависимость константы равновесия реакции 2C 3 H 6 (г) = C 2 H 4 (г) + C 4 H 8 (г) от температуры между 300 К и 600 К описывается уравнением
CO 2 (г) + C(тв) = 2CO(г)
содержится 17% (по объему) CO 2 . Сколько процентов CO 2 будет содержаться в газе при общем давлении 20 атм? При каком давлении в газе будет содержаться 25% CO 2 ?
H 2 O(г) = H 2 (г) + 1/2O 2 (г) при этих условиях.
CO(г) + H 2 O(г) = CO 2 (г) + H 2 (г)
при 500 o C равна K p = 5.5. Смесь, состоящая из 1 моль CO и 5 моль H 2 O, нагрели до этой температуры. Рассчитать мольную долю H 2 O в равновесной смеси.
N 2 O 4 (г) = 2NO 2 (г)
при 25 o C равна K p = 0.143. Рассчитать давление, которое установится в сосуде объемом 1 л, в который поместили 1 г N 2 O 4 при этой температуре.
I 2 (г) = 2I (г).
при 250 o C r G o = –2508 Дж. моль –1 . При каком общем давлении степень превращения PCl 5 в PCl 3 и Cl 2 при 250 o C составит 30%?
2HI(г) = H 2 (г) + I 2 (г)
константа равновесия K P = 1.83 10 –2 при 698.6 К. Сколько граммов HI образуется при нагревании до этой температуры 10 г I 2 и 0.2 г H 2 в трехлитровом сосуде? Чему равны парциальные давления H 2 , I 2 и HI?
PCl 5 (г) = PCl 3 (г) + Cl 2 (г)
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K равна K P = 6.09 10 –3 . Рассчитать общее давление, необходимое для получения метанола с 90% выходом, если CO и H 2 взяты в соотношении 1: 2.
CO(г) + 2H 2 (г) = CH 3 OH(г)
находится в равновесии при 500 K и 10 бар. Если газы идеальные, как повлияют на выход метанола следующие факторы: а) повышение T ; б) повышение P ; в) добавление инертного газа при V = const; г) добавление инертного газа при P = const; д) добавление H 2 при P = const?
2NOCl(г) = 2NO(г) + Cl 2 (г)
устанавливается при 227 o C и общем давлении 1.0 бар, когда парциальное давление NOCl равно 0.64 бар (изначально присутствовал только NOCl). Рассчитать r G o для реакции. При каком общем давлении парциальное давление Cl 2 будет равно 0.10 бар?
N 2 (г) + 3H 2 (г) = 2NH 3 (г)
при 400 o C равна K = 1.60 10 –4 .
PCl 5 (г) = PCl 3 (г) + Cl 2 (г).
Чему будет равна степень диссоциации PCl 5 , если в систему добавить N 2 , чтобы парциальное давление азота было равно 0.9 атм? Общее давление поддерживается равным 1 атм.
N 2 (г) + O 2 (г) = 2NO(г)
K p = 2.5 10 –3 . В равновесной смеси N 2 , O 2 , NO и инертного газа при общем давлении 1 бар содержится 80% (по объему) N 2 и 16% O 2 . Сколько процентов по объему составляет NO? Чему равно парциальное давление инертного газа?
ln K = –1.04 –1088 /T +1.51 10 5 /T 2 .
